自然界中有没有非生命物质表现出生命体的特征?

有。生命与非生命没有绝对清晰的界限,休眠的微生物、休眠的动物、病毒、亚病毒因子不时被一些来源称为介于生命与非生命之间。
科普中国在 2025 年翻译并发布了 Phil Jaekl 的文章 The Animals That Exist Between Life and Death,谈论了轮虫、鳗虫等动物在脱水休眠后加水恢复的历史研究,谈论了关于这休眠是死是活还是第三种状态的争议。
黏土中的硅酸盐结晶可以合并水中溶解的硅酸盐而生长,在风、水等影响下改变形态,特定的结晶形态更容易在河床中堆积并促使更多结晶形成;在水位下降露出河床时,一些结晶会被风吹到其他地方并重复堆积过程。Cains-Smith 在 1982 年提出黏土结晶可以储存晶体结构缺陷、错位、离子置换等信息并进行复制[1]。
自然形成的有机分子可以在黏土结晶的硅酸盐表面上发生化学反应。
现代深海热泉的自然环境在自发进行耐环境微生物体内进行的 90% 以上的化学反应并产生氢气。
看起来,原始地球上的一些粒子在太阳辐射等影响下发生化学反应,一些产物积累起来、形成自我维持的化学反应网络,一些分子发生了自我制造过程,多种分子结合、形成特定的耗散系统。在适当的热力学自由能支持下,这些耗散系统能够相对稳定地、高密度地储存若干信息,能够将储存的信息用于新陈代谢,能够在自我制造的过程中发生各种错误、经历广义自然选择,将熵和废热排放到太空。四十多亿年后,这些耗散系统的若干后代将其追认为生命。从非生命到生命的过程包含许多模糊的部分,里面大概会有许多如题述地表现出生命特征的非生命。相关研究还在进行中。
2025 年 5 月发表的一篇文章称,在酸性的水中加热 RNA,可以有效地分离双链 RNA;那之后将溶液的酸性中和并冷冻,在冰晶间的液态微区里,三核苷酸三磷酸(三联体 RNA)会覆盖单链 RNA、防止它们重新结合成双链 RNA,这些三联体可以作为 5TU/t1 聚合酶核酶(体外进化产生的核酶,材料是 RNA,可用 RNA 二联体、三联体作为底物)进行 RNA 复制的底物。经过反复的冻融循环,在酸碱度、温度、浓度梯度的作用下,RNA 可以持续地由 RNA 催化进行复制,随机引物与底物搞出了新的序列,催化所用的 5TU/t1 聚合酶核酶亦可在这种条件下复制自己的一些片段。
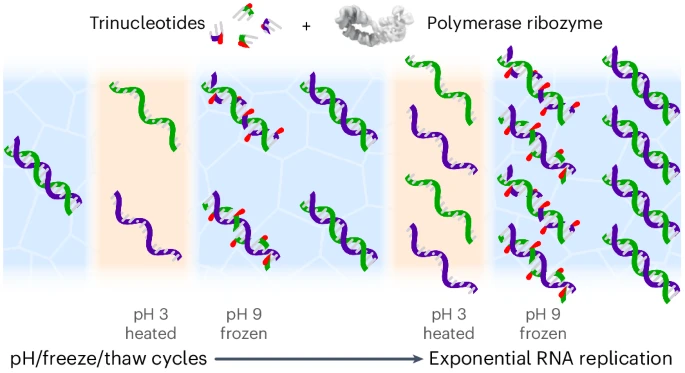
- 在原始地球上,昼夜交替、灼热岩石与低温大气的交界等会提供上述条件。当代地球上就存在火山与冰共存的场景[2]。考虑到 RNA 的浓度和冻融循环的难度,淡水比海水更适合进行上述操作。干湿交替也能提高 RNA 浓度并从其他物质产生 RNA,但干湿交替可能影响 RNA 链的稳定性。
- pH 低于 4 的酸性条件可以让 RNA 双链分离需要的温度从中性条件的约 66 摄氏度下降到低于 40 摄氏度[3]。
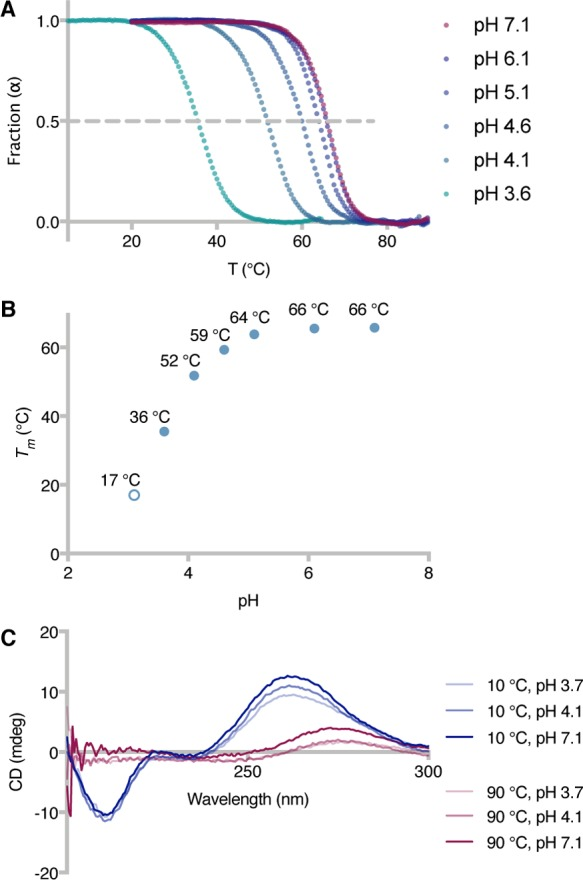
今后,进一步研究大概会找到更擅长进行自我复制的 RNA,找到用原始地球的条件产生这种 RNA 的过程。
在现有的关于化学进化的实验里,最简单的自我制造分子是亚氨基二乙酸[4]。
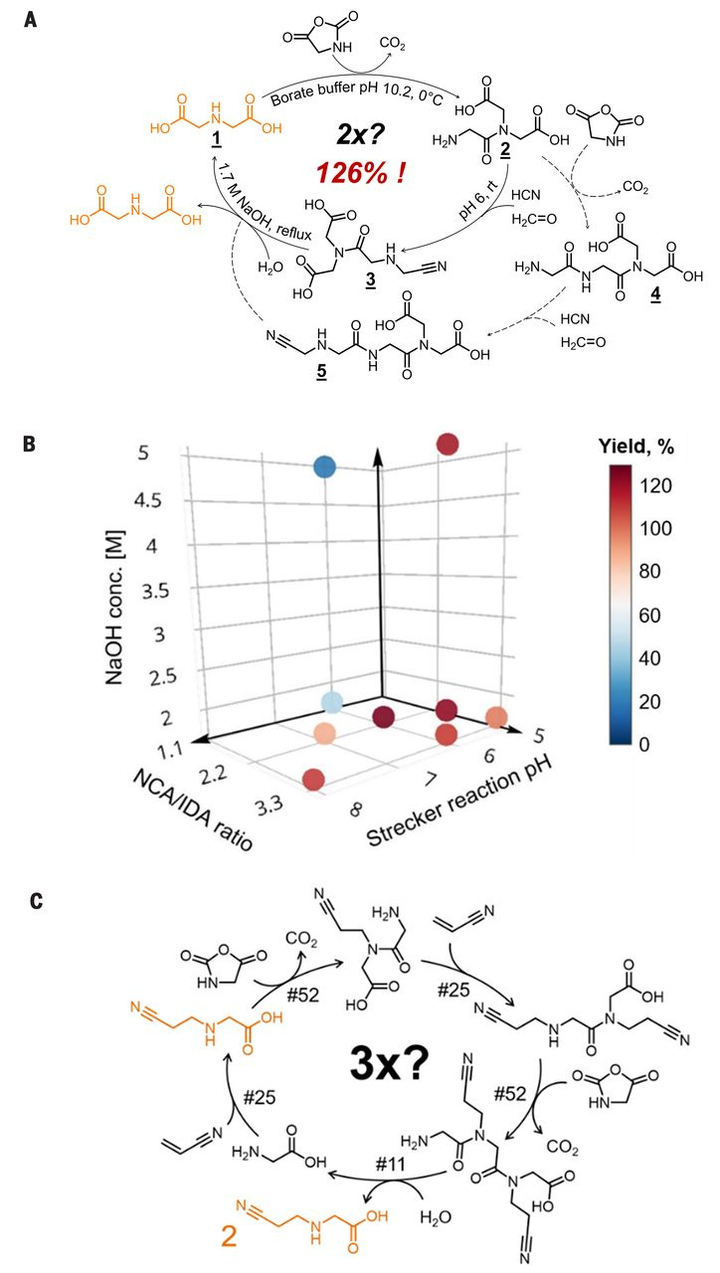
看起来,核苷酸可以在远古地球上存在的被太阳紫外线照射、干湿交替的陆地水潭之类环境自然产生。可以参考我回答过的:帮孩子问:生命起源是从海水开始还是淡水?
实验显示,核苷三磷酸可以在镁铁火山玻璃上自组织成 RNA 链[5]。如此形成的 RNA 链长约 90 到 150 个核苷酸。这达到 2012 年 Joyce 提出的进行演化需要的可能长度(50 到 5000 个核苷酸)。
- 镁铁火山玻璃存在于冥古宙地球、诺亚纪火星。火山活动、天体撞击都可以参与它们的形成和变化,并提供一些热量。动力学数据显示,小撞击坑里数吨破碎且浸水的火山玻璃在材料充足时每天可以合成近 1 克 RNA。
- 存在其他自组织成链的方法。
持续潮湿的环境对蛋白质、核酸链等并不友好。地球生物的自然起源可能需要时常干湿交替的浅水或陆地,或是靠岩石微区室提供遮蔽。
- 对于浅水,在水体干燥时,脂质可以自组装为囊泡,这可能包裹了 RNA 等分子、成为细胞的起源。可以参考实验[6]。
- 对于深水,在 70 摄氏度、pH 大于 12 的条件下,脂肪酸可以自组织为囊泡[7]。
关于有机化合物的出现:
在实验室,萨瑟兰和其他科学家加热简单的碳基化学物质,用紫外线照射并间歇性地干燥它们,产生了 RNA、DNA、蛋白质等[8][9][10]。化学家尚未在模拟海水的条件下合成如此多样化的生物分子,大量的水和远比钾多的钠对这些分子不利。地球生物可能起源于反复干涸的浅海与池塘。这有助于太阳辐射影响生物分子的手性偏差。
2025 年,一篇文章提出,水雾中的带电水滴之间的放电可以诱发小规模化学反应来制造有机分子。这些水滴落在岩石上,有机分子会积累在岩石缝隙里、经历干湿交替。这需要的水深接近零。
水滴在空气中破裂或受到冲击、振动后发生电荷分离并带电的现象由菲利普·勒纳德第一个进行科学描述,后称勒纳德效应。通常情况下,较小的水滴带负电,较大的水滴带正电。这些水滴间可以发生微小的放电现象。
实验显示,将水滴喷入甲烷、二氧化碳、氨气、氮气组成的混合气体里,可以靠上述微小放电形成具有碳 - 氮键的有机分子。
https://doi.org/10.1126/sciadv.adt8979
水微滴的气液界面、固液界面具有与体相水不同的热力学性质,能够进行一些和体相水不同的化学反应,能够将体相水中的一些化学反应加速四个数量级,能够自发进行一些氧化还原反应、产生一些高反应性的分子并为其他反应提供能量。在原始地球上,这可能有助于一些有机分子的产生。
可以看看关于水微滴产生过氧化氢的文章:
Bogot, A.; Poline, M.; Ji, M.; Dochain, A.; Simonsson, A.; Rosén, S.; Zettergren, H.; Schmidt, H. T.; Thomas, R. D.; Strasser, D. The mutual neutralization of hydronium and hydroxide. Science 2024, 383, 285.
Asserghine, A.; Baby, A.; N’Diaye, J.; Romo, A. I. B.; Das, S.; Litts, C. A.; Jain, P. K.; Rodríguez-López, J.
Dissolved Oxygen Redox as the Source of Hydrogen Peroxide and Hydroxyl Radical in Sonicated Emulsive Water Microdroplets. J. Am. Chem. Soc. 2025, DOI:10.1021/jacs.4c16759